|
单核细胞及由单核细胞演变而来的具有吞噬功能的巨噬细胞,称为单核吞噬细胞系统。单核细胞发生于骨髓的多能干细胞,循环于血液中,穿透血管内皮进入组织内,转变为巨噬细胞。单核吞噬细胞系统在体内分布广,细胞数量多,主要分布于疏松结缔组织、肝、脾、淋巴结、骨髓、脑、肺以及腹膜等处。
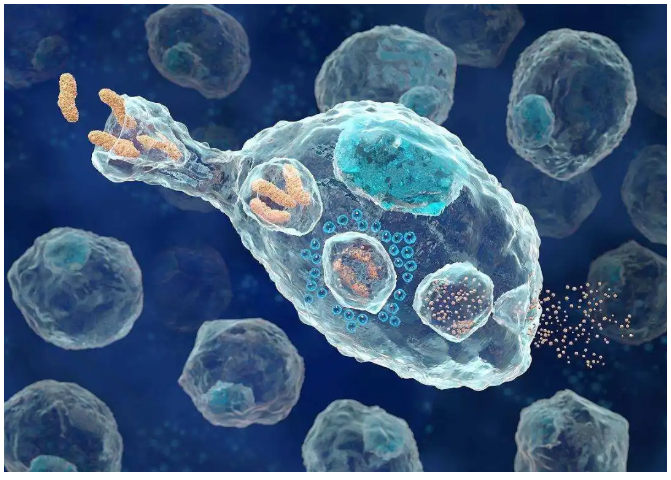
极化形式
巨噬细胞是广泛分布的先天免疫细胞,在各种生理和病理过程中起着不可或缺的作用,包括器官发育,宿主防御,急性和慢性炎症以及组织稳态和重塑。巨噬细胞存在两种极化形式: 经典活化巨噬细胞(M1)和替代性活化巨噬细胞(M2)。 M1型巨噬细胞由Th1细胞因子(TNF-α、IFN-γ)和细菌成分(脂多糖等)诱导。活化的M1巨噬细胞吞噬并破坏微生物,清除肿瘤细胞,并将抗原呈现给T细胞以引起适应性免疫反应。因此,它们在抵御病原体方面发挥着重要作用。M1型巨噬细胞释放高水平的促炎细胞因子,如TNF-α, IL-6和IL-1β,从而促进Th1应答。
M2的激活是对IL-4、IL-10和IL-13刺激的响应。它们表现出更强的免疫抑制表型,其特征是T细胞抗原呈递减少和刺激Th2反应的细胞因子的产生。不同的刺激因子可诱导不同亚型的M2巨噬细胞。M2型巨噬细胞可进一步分为:M2a、M2b、M2c、M2d。
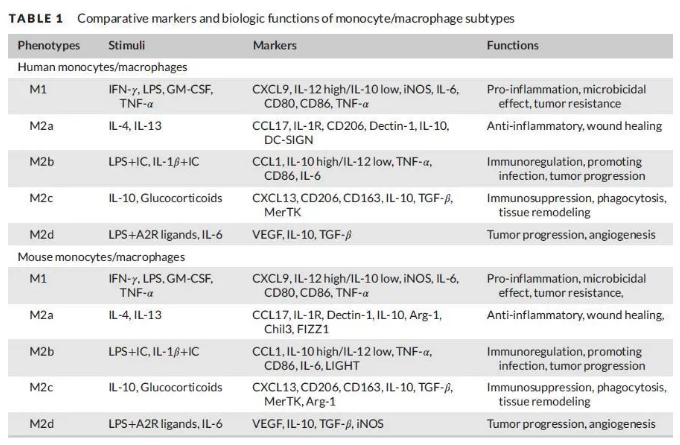 A2R, A2adenosine receptor; Arg-1, arginase-1; CCL, chemokine (C-C motif) ligand; CD, cluster of differentiation; Chil3, chitinase-like 3; CXCL, chemokine (CX-Cmotif) ligand;DC-SIGN, dendritic cell-specific intercellular adhesionmolecule-3-grabbing non-integrin; FIZZ1, found in inflammatory zone 1; IC, immune complex; LIGHT, homologous to lymphotoxin, inducible expression, competes with herpes simplex virus (HSV) glycoprotein D for binding to HSV entry mediator, a receptor expressed on T lymphocytes; iNOS, inducible nitric oxide synthase; MerTK, Mer receptor tyrosine kinase; VEGF, vascular endothelial growth factor. A2R, A2adenosine receptor; Arg-1, arginase-1; CCL, chemokine (C-C motif) ligand; CD, cluster of differentiation; Chil3, chitinase-like 3; CXCL, chemokine (CX-Cmotif) ligand;DC-SIGN, dendritic cell-specific intercellular adhesionmolecule-3-grabbing non-integrin; FIZZ1, found in inflammatory zone 1; IC, immune complex; LIGHT, homologous to lymphotoxin, inducible expression, competes with herpes simplex virus (HSV) glycoprotein D for binding to HSV entry mediator, a receptor expressed on T lymphocytes; iNOS, inducible nitric oxide synthase; MerTK, Mer receptor tyrosine kinase; VEGF, vascular endothelial growth factor.
组织中的巨噬细胞
巨噬细胞存在于所有组织内,按照特定的模式,每种组织中的巨噬细胞均有不同。组织常驻巨噬细胞在其形态,转录谱,解剖学位置和功能能力方面表现出极大的多样性。常驻巨噬细胞通过充当哨兵并响应生理变化以及来自外部的刺激来调节组织的动态平衡。
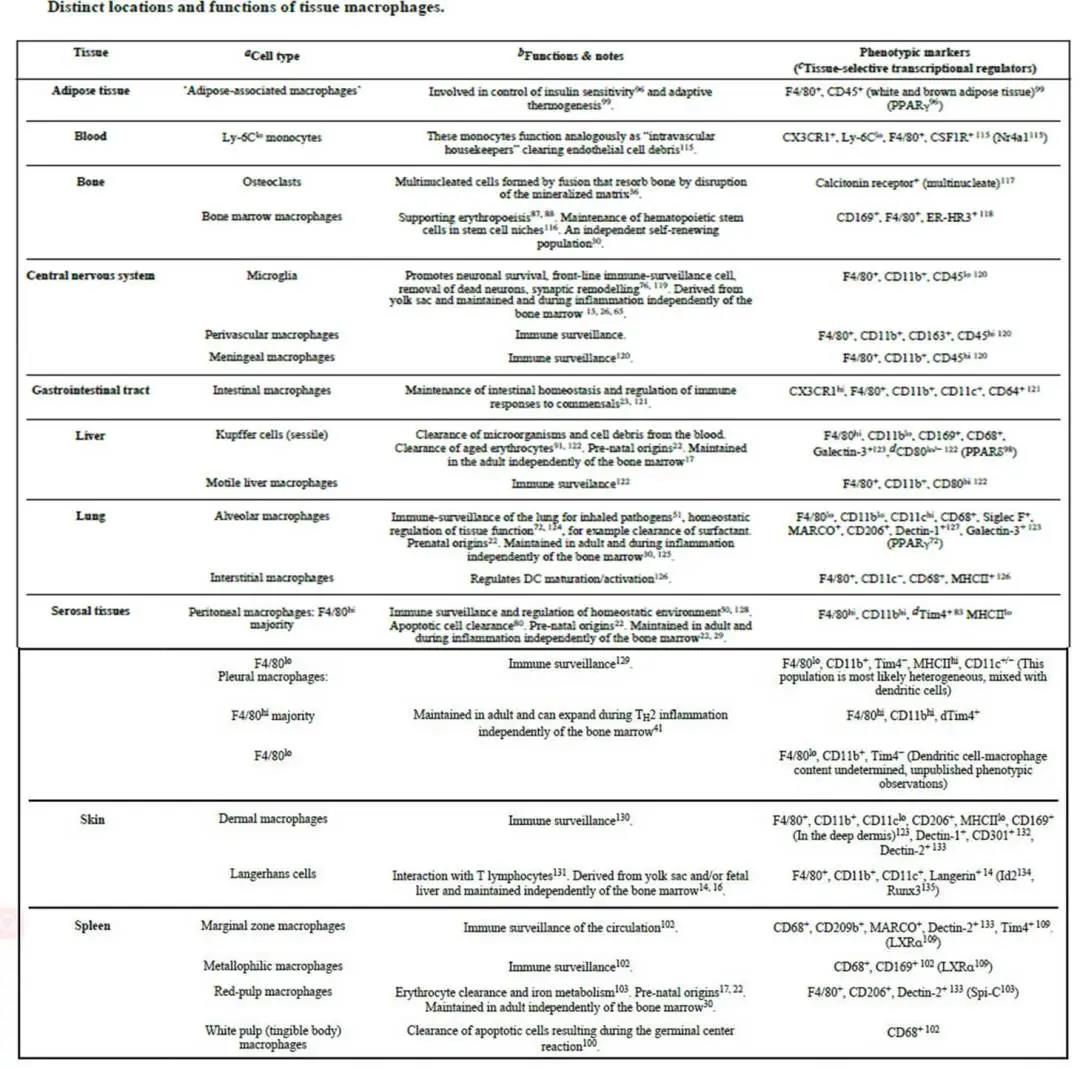 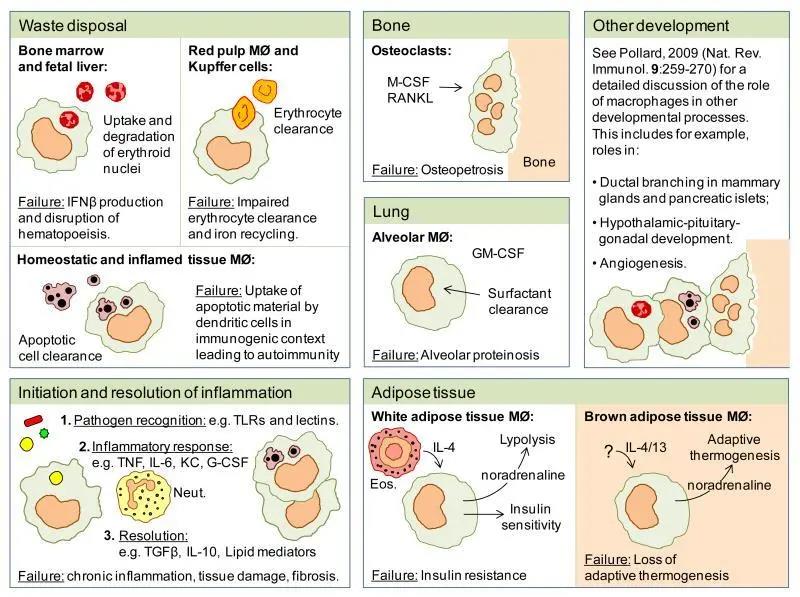
组织驻留巨噬细胞的功能。驻留在组织中的巨噬细胞在清除(红细胞核,衰老的红细胞,凋亡细胞和肺表面活性物质的降解),发育(骨骼降解和血管生成)和代谢调节(调节胰岛素敏感性和脂肪组织的适应性热生成)中具有广泛的作用。它们还起着免疫哨兵的基本作用,引发炎症反应,清除炎症碎片并恢复稳态组织环境。
脂肪组织
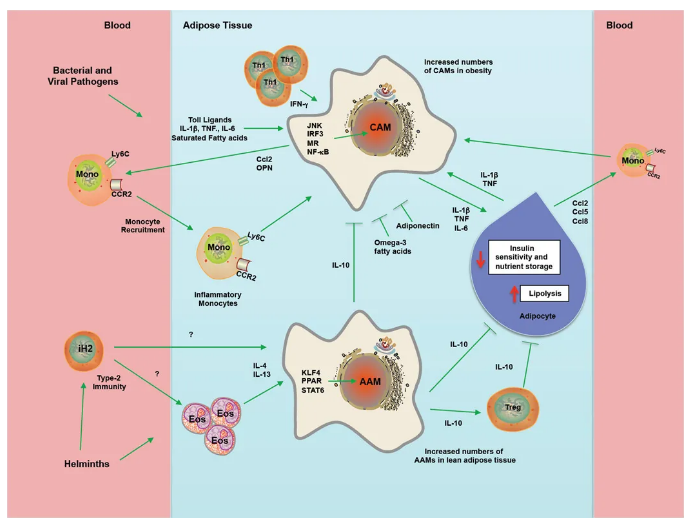
在肥胖中,M1和M2型巨噬细胞不同地调节胰岛素敏感性。在瘦弱的健康动物中,脂肪组织巨噬细胞占基质细胞的10% -15%,M2型巨噬细胞通过IL-10的产生对维持脂肪细胞中的胰岛素敏感性至关重要。2型细胞因子如IL-4和IL-13来自多种细胞,包括嗜酸性粒细胞,对维持组织中AAM表型很重要。相反,在肥胖期间,Ly6Chi单核细胞被招募,巨噬细胞的含量增加到45% - 60%。与正常的常驻巨噬细胞相比,这些巨噬细胞表达了一种炎症表型,,其特征在于TNF-α,IL-6和IL-1β的产生。这些炎性巨噬细胞降低了胰岛素敏感性,同时促进了多余营养的储存。增大的白色脂肪组织反过来释放趋化因子,例如CCL2,CCL5和CCL8,以募集额外的Ly6Chi炎性单核细胞,进一步加剧了这一过程。在细菌和病毒感染期间,该机制也得到了增强,因此必需营养素被转移至淋巴细胞,淋巴细胞必须利用糖酵解来增强其在压力时的活化。
肿瘤组织
浸润肿瘤微环境的巨噬细胞通常被称为肿瘤相关巨噬细胞(TAM)。TAM渗透,与许多癌症预后不良相关,提示它们促进肿瘤进展。实际上,TAM可以刺激肿瘤细胞的增殖,侵袭,转移,促进血管生成并抑制抗肿瘤反应。抗肿瘤活性差是IL-10,TGF-β和前列腺素E2(PGE2)产生更高以及炎性细胞因子(如TNF-α和IL-6)合成减少的结果。此外,TAMs表现出较差的抗原呈递能力,从而导致T细胞的活化和增殖受到抑制。
TAMs来自循环单核细胞,这些单核细胞被基质细胞和肿瘤细胞产生的几种生长因子,尤其是趋化因子募集到肿瘤中。除了M-CSF外,CCL2,CCL3,CCL4和CCL5是肿瘤巨噬细胞群体公认的趋化因子。研究发现,一旦巨噬细胞进入肿瘤微环境,相应的CCR2就被下调。提示受体下调是一种在肿瘤微环境中捕获募集的巨噬细胞的机制。此外,在结肠癌模型中,CCL20 / LARC趋化分化为TAM的单核细胞。在人类乳腺癌模型中,CCL18与CSF-2协同参与了单核细胞的动员和募集。VEGF-A被鉴定为体内异种移植模型中的巨噬细胞募集因子,可能通过诱导化学吸引剂间接发挥作用。
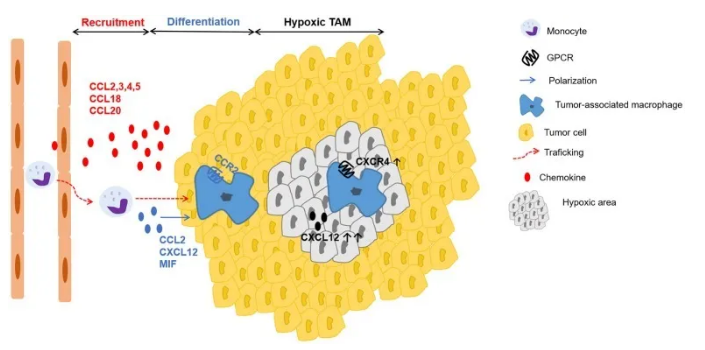
参与TAM募集,分化和定位的趋化因子的示意图。趋化因子CCL2,CCL3,CCL4,CCL5,CCL18,CCL20等肿瘤衍生因子会主动向肿瘤中募集单核细胞(红色箭头),并分化为肿瘤相关巨噬细胞(TAM)。趋化因子CCL2,CXCL12和趋化因子样蛋白MIF在TAM极化中的特殊作用(蓝色箭头)。在低氧区域,巨噬细胞上较高的CXCL12量和CXCR4的表达增加,会在低氧张力下增强向这些特定部位的迁移和保留。
产品推荐
单/多因子检测
| 种属 |
检测方向 |
货号 |
检测因子 |
| Human |
Chemokine |
LX-171AK99MR2 |
6Ckine/CCL21,BCA-1/CXCL13,CTACK/CCL27,ENA-78/CXCL5,Eotaxin/CCL11,Eotaxin-2/CCL24,Eotaxin-3/CCL26,Fractalkine/CX3CL1,GCP-2/CXCL6,GM-CSF,Gro-α /CXCL1,Gro-β/CXCL2,I-309/CCL1,IFN-I,IL-18,IL-2,IL-4,IL-6,IL-8/CXCL 8,IL-10,IL-16,IP-10/CXCL 10,I-TAC /CXCL11,MCP-1 /CCL2,MCP-2 /CCL8,MCP-3 /CCL7,MCP-4 /CCL13,MDC/CCL 22,MIF,MIG/CXCL19,MIP-1α/CCL3,MIP-1δ/CCL15,MIP-3a/CCL20,MIP-3β/CCL19,MPIF-1/CCL23,SCYB16/CXCL 16,SDF-1α+β/CXCL12,TARC/CCL17,TECK/CCL25,TNF-α |
| Human |
Cytokine/ Th1/Th2 |
LX-M5000005L3 |
GM-CSF, IFN-γ, IL-2, IL-4, IL-5, IL-10, IL-12 (p70), IL-13, TNF-α |
| Human |
Chemokine |
LX-LKTM012 |
CCL2/JE/MCP-1,CCL3/MIP-1 alpha,CCL4/MIP-1 beta,CCL5/RANTES,CCL11/Eotaxin,CXCL1/GRO alpha/KC/CINC-1,CXCL10/IP-10/CRG-2,IL-8/CXCL8 |
| Human |
Cytokine/Chemokine |
LX-HCYTOMAG-60K-41 |
EGF,Eotaxin/CCL11,FGF-2/FGF-basic,Flt3 Ligand,Fractalkine/CX3CL1,G-CSF,GM-CSF,GRO,IFNα2,IFNγ,IL-1α,IL-1β,IL-1Ra,IL-2,IL-3,IL-4,IL-5 ,IL-6,IL-7,IL-8/CXCL8,IL-9,IL-10,IL-12 (p40),IL-12 (p70),IL-13,IL-15,IL-17A/CTLA8,IP-10/CXCL10,MCP-1/CCL2,MCP-3/CCL7,MDC/CCL22,MIP-1α/CCL3,MIP-1β/CCL4,PDGF-AA,PDGF-AB/BB,RANTES/CCL5,TGFα,TNFα,TNFβ/Lymphotoxin-α(LTA),VEGF-A |
| Human |
Cytokine/Chemokine |
LX-HCYP2MAG-62K-23 |
6Ckine/CCL21/Exodus-2,BCA-1/CXCL13,CTACK/CCL27,ENA-78/CXCL5,Eotaxin-2/CCL24/MPIF-2,Eotaxin-3/CCL26,I-309/CCL1,IL-16,IL-20,IL-21,IL-23,IL-28A/IFNλ2,IL-33/NF-HEV(mature),LIF,MCP-2/CCL8,MCP-4/CCL13,MIP-1δ/MIP-5/CCL15,SCF,SDF-1/CXCL12,TARC/CCL17,TPO,TRAIL/TNFSF10, TSLP |
| Human |
Cytokine/Chemokine |
LX-HCYP3MAG-63K-11 |
HCC-1/CCL14,IL-11,IL-29/IFNλ1,I-TAC/CXCL11,LIX/CXCL6/GCP-2,Lymphotactin/XCL1,M-CSF,MIG/CXCL9,MIP-3α/CCL20,MIP-3β/CCL19,NAP-2/CXCL7 |
| Human |
Cytokine/Chemokine |
LX-HCYP4MAG-64K-20 |
BAFF/Blys,BRAK/CXCL14,CCL28,CXCL16,HCC-4/CCL16,HMGB1,IFNβ,IL-14/α-Taxilin,IL-19,IL-24,IL-28B/IFNλ3,IL-32α,IL-34,IL-35, IL-36β/IL-1F8,IL-37/IL-1F7,IL-38/IL-1F10,MIP-4/PARC/CCL18,MPIF/CCL23,YKL40/CHI3L1 |
| Human |
Diabetes |
LX-171A7001M |
C-Peptide, Ghrelin, GIP, GLP-1, Glucagon, Insulin, Leptin, PAI-1, Resistin, Visfatin |
| Human |
GLP-1 Active |
LX-K1503OD-1 |
GLP-1 (active) |
| Human |
GLP-1 Total |
LX-K1503PD-1 |
GLP-1 Total |
| Human |
Cancer |
HCCBP1MAG-58K |
α-Fetoprotein (AFP),CA125,CA15-3,CA19-9,CEA,CYFRA21-1,sFAS/TNFRSF6,sFasL, FGF-2/FGF-basic,HCGβ,HE4,HGF,IL-6,IL-8/CXCL8,Leptin,MIF,Osteopontin (OPN),Prolactin,PSA (free),PSA (total),SCF,TGFα,TNFα,TRAIL/TNFSF10,VEGF-A |
| Human |
Cancer |
HCCBP2MAG-58K |
Antithrombin III,Complement Factor H (CFH),Extracellular Matrix Protein 1 (ECM1),Vitamin D Binding Protein |
| Human |
Cancer |
HCCBP3MAG-58K |
Cathepsin D,Ferritin, Fibroblast Activation Protein (FAP),Galectin 3,IGFBP3,Melanoma Inhibitory,Activity (MIA),Myeloperoxidase(MPO),Sex Hormone Binding Globulin (SHBG) |
| Human |
Cancer |
HCCB4MAG-58K |
ALDH1A1,Carbonic Anhydrase 9 (CA9),CD44,EpCAM,Hepsin,Kallikrein-6,Mesothelin,Midkine,NCAML1/L1CAM/,CD171,Transglutaminase 2(TGM2) |
| Human |
Cancer |
HCMBMAG-22K |
DKK1,GDF-15,Neuron-specific,Enolase (NSE),Osteonectin/SPARC, Osteoprotegerin(OPG),Periostin, TRAP5,TWEAK,YKL40/1CHI3L1 |
| Human |
Cancer |
HAGP1MAG-12K |
Angiopoietin-2,BMP-9,EGF,Endoglin,Endothelin-1,FGF-1/FGF-acidic,FGF-2/FGF-basic,Follistatin (FST),G-CSF,HB-EGF,HGF,IL-8/CXCL8,Leptin,Placental Growth Factor (PLGF),VEGF-A,VEGF-C,VEGF-D |
| Human |
Cancer |
HANG2MAG-12K |
Angiostatin/Kringle,sAXL,sCD31/sPECAM-1,sc-Kit/sStem Cell Factor Receptor (SCFR),sE-Selectin,sEGFR/sHER1/sErbB1,sHER2/sEGFR2/, sErbB2,sHER3/sEGFR3/sErbB3,sHGFR/sc-Met,sIL-6Rα,sNeuropilin-1 (sNRP-1),Osteopontin (OPN),PDGF-AB/BB,Tenascin C (TN-C),Thrombospondin-2(TSP-2),sTIE-2,suPAR,sVEGFR1/sFlt-1,sVEGFR2/sKDR/sFlk-1,sVEGFR3/sFlt-4 |
参考文献
[1]Le xun Wang, Sheng xi Zhang, Hui juan Wu, Xiang lu Rong, Jiao Guo. M2b macrophage polarization and its roles in diseases. J Leukoc Biol. 2019 Aug; 106(2): 345–358.
[2]Luke C. Davies, Stephen J. Jenkins, Judith E. Allen, Philip R. Taylor. Tissue-resident macrophages. Nat Immunol. Author manuscript; available in PMC 2014 Jun 4.
[3]Thomas A. Wynn, Ajay Chawla, Jeffrey W. Pollard. Origins and Hallmarks of Macrophages: Development, Homeostasis, and Disease. Nature. 2013 Apr 25; 496(7446): 445–455.
[4]Pieter Ruytinx, Paul Proost, Jo Van Damme, Sofie Struyf. Chemokine-Induced Macrophage Polarization in Inflammatory Conditions. Front Immunol. 2018; 9: 1930.
|
