本周为大家带来的文献为发表于Int Immunopharmacol. (IF: 5.6)的” Experimental evidence for alpha enolase as one potential autoantigen in the pathogenesis of both autoimmune thyroiditis and its related encephalopathy”。本文使用了LabEx提供的Luminex检测服务。
自身免疫性甲状腺炎是一种多因素紊乱疾病,其特征包括抗甲状腺炎抗体高表达和本地淋巴浸润。AIT相关脑病,也被称为桥本脑病(HE),是一种重要的甲状腺外自身免疫要素,其中有中枢神经系统损害和功能障碍参与。自身免疫性甲状腺炎的病人血清中ENO1Ab 滴度较高。本文旨在探讨ENO1Ab是否是甲状腺和大脑中的致病抗体。免疫甲状腺球蛋白(Tg)的小鼠血清中ENO1Ab滴度明显升高。免疫了ENO1的小鼠血清中TgAb和促甲状腺激素(TSH)的水平都明显升高。在ENO1免疫小鼠的甲状腺中观察到明显的CD16+细胞浸润、IgG沉积和caspase-3裂解。ENO1免疫小鼠的空间学习记忆能力和突触功能受损。此外,ENO1免疫小鼠脑中Iba-1、GFAP、interlukin-6、CDK5和磷酸化tau的表达水平升高,内皮紧密连接蛋白降低。这些结果表明,ENO1Ab可通过ADCC效应导致甲状腺细胞损伤,并通过破坏血脑屏障损害脑功能。
LabEx提供的Luminex检测服务:
蛋白芯片用于筛选W10时脑组织中细胞因子的产生。结果显示,ENO1组大脑皮层和海马组织匀浆上清液中IL-5、IL-6和IL-12的表达水平分别比CON组平均高2.41倍、2.39倍和2.61倍(图9D),而其他40种细胞因子的分泌似乎没有改变。
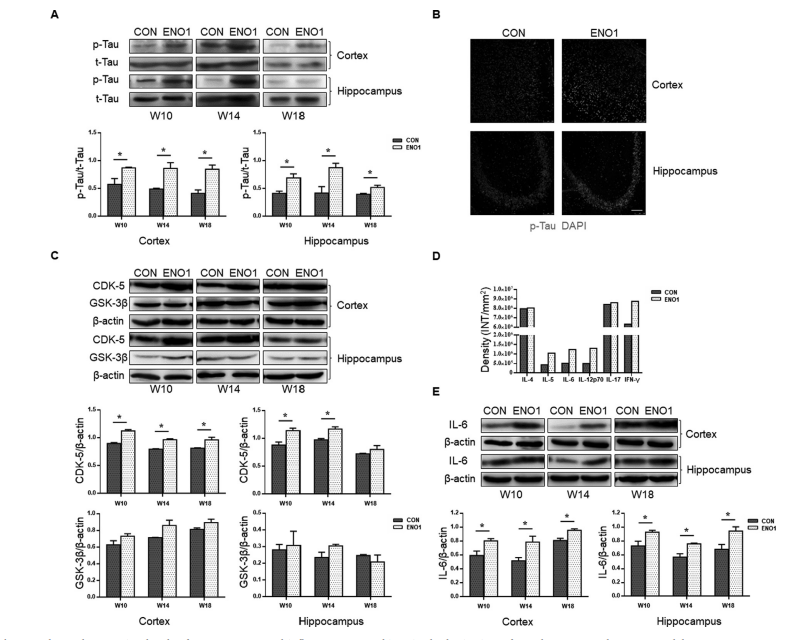
H-ENO1Ab小鼠模型脑组织中 p-Tau、CDK-5 和炎症细胞因子的表达水平升高。
重要发现:
ENO1在自身免疫性甲状腺炎中的作用:在实验性自身免疫性甲状腺炎(EAT)模型中,免疫小鼠的血清中ENO1特异性IgG及其四种亚型(IgG1、IgG2a、IgG2b、IgG3)显著增加,尤其是IgG2a和IgG1。ENOl免疫也导致血清甲状腺球蛋白抗体(TgAb)水平和甲状腺内单核细胞浸润评分显著增加。
异位抗原与自身免疫反应:研究发现甲状腺球蛋白(Tg)与ENO1具有10处同源性,暗示ENO1不仅作为甲状腺和脑组织之间的共同抗原,还可能通过表位模拟和分子间表位扩展在自身免疫反应中发挥作用。
高ENO1Ab小鼠模型研究:在高ENO1Ab小鼠模型中,血清ENO1特异性IgG及其亚型显著增加,脾脏中Th1/Th2和Th17/Treg细胞典型细胞因子的mRNA表达水平增加。特别是IL-4和IL-17A mRNA的表达与血清IgG亚型的分布一致。
甲状腺和脑组织损伤机制:在高ENO1Ab小鼠模型中,甲状腺组织中可见IgG沉积、CD16+细胞聚集和细胞凋亡增加,推测ENO1Ab可能通过抗体依赖的细胞介导细胞毒作用(ADCC)损伤甲状腺细胞,导致甲状腺激素分泌不足和促发其他甲状腺自身抗体的产生。
脑组织损伤与认知功能障碍:高ENO1Ab小鼠模型中,海马和皮质中过度磷酸化的Tau蛋白表达增加,伴随微血管周围水肿和血脑屏障(BBB)功能障碍,导致小胶质细胞和星形胶质细胞激活,促炎性细胞因子(如IL-6)表达增加,最终导致认知和行为损害。
潜在机制总结:ENO1Ab通过损伤脑微血管内皮细胞,导致BBB通透性增加,周围水肿,胶质细胞激活,脑内IL-6水平上调,CDK-5表达增加,Tau蛋白磷酸化增强,最终导致认知和行为功能障碍。







 沪公网安备31011502400759号
沪公网安备31011502400759号
 营业执照(三证合一)
营业执照(三证合一)


