新年伊始,我们都将要结束一年的辛勤工作,将疫情和病毒甩在脑后,回到家乡同亲友享受七天长假。而在漫长的回乡路上,中和抗体正在悄悄保护我们免受新冠病毒侵扰。
什么是中和抗体?
中和抗体(NAb)由骨髓中的B细胞产生。为了阻止病原体感染人体,中和抗体发展出了不同的针对策略:1)包膜病毒:阻止病毒附着,进入细胞;2)非包膜病毒:替代宿主细胞与病毒衣壳蛋白结合;3)细菌:阻止毒素的有害作用。当病原体被“中和”后,就会被白细胞降解,再由脾脏过滤病原体,然后排出体外。
新冠病毒表面有不同的蛋白:膜蛋白(M)、包膜蛋白(E)以及刺突蛋白(S)。中和抗体主要通过与刺突蛋白的受体结合域(RBD)相互作用来阻止病毒与血管紧张素转换酶2(ACE2)受体(ACE2)的结合。
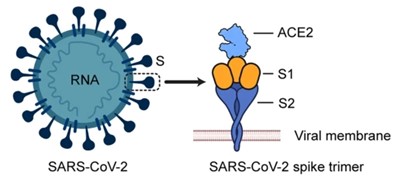
图1. SARS-COV-2 结构图
如何检测中和抗体?
中和抗体可以被用于医疗目的,包括血清疗法,疫苗接种等。它还可以反映群体的感染率、个人的康复情况以及疫苗的效果。当下,已研发出多种检测中和抗体的方法:
1. 蚀斑减少中和试验(PRNT)
PRNT通过将待测抗体的血清样品稀释液和病毒悬浮液混合,进行孵育使抗体和病毒发生反应。再将混合液倒在单层宿主细胞上,形成斑块。可以通过斑块形成单位的浓度估计病毒中抗体的滴度。这个方法仍旧是血清测试和确认免疫保护的金标准,但因为PRNT的产量较低(只能在6孔或者24孔板上实验),且对实验技术高要求,所以不适用于大规模血清测试和疫苗评估。
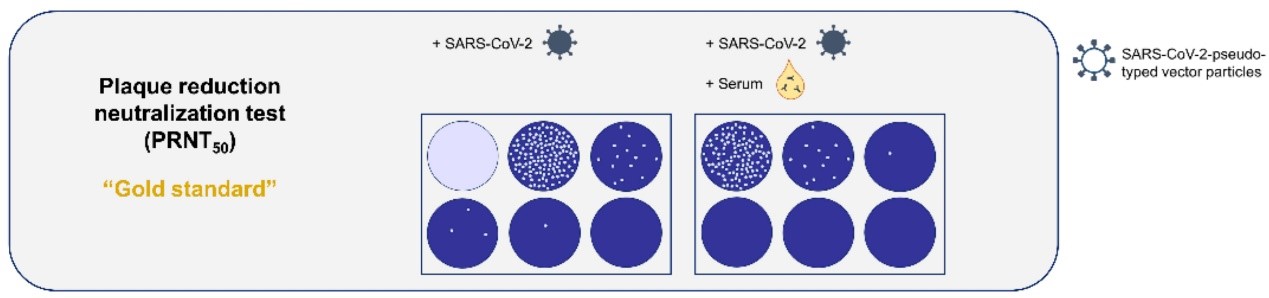
图2. 蚀斑减少中和试验
2. 微中和检测(microneutralization assay,MNA)
MNA基于PRNT研发,但克服了后者的缺点——低通量(图3)。实验通常在96孔板上进行,使用免疫染色可视化感染区域,再由成像器计数。MNA可以在3天内完成实验,而PRNT需要一周。同时自动化的流程帮助MNA提高了读数的准确性和客观性。但PRNT和MNA都需要在生物安全三级实验室中进行,因此对实验环境有一定需求。
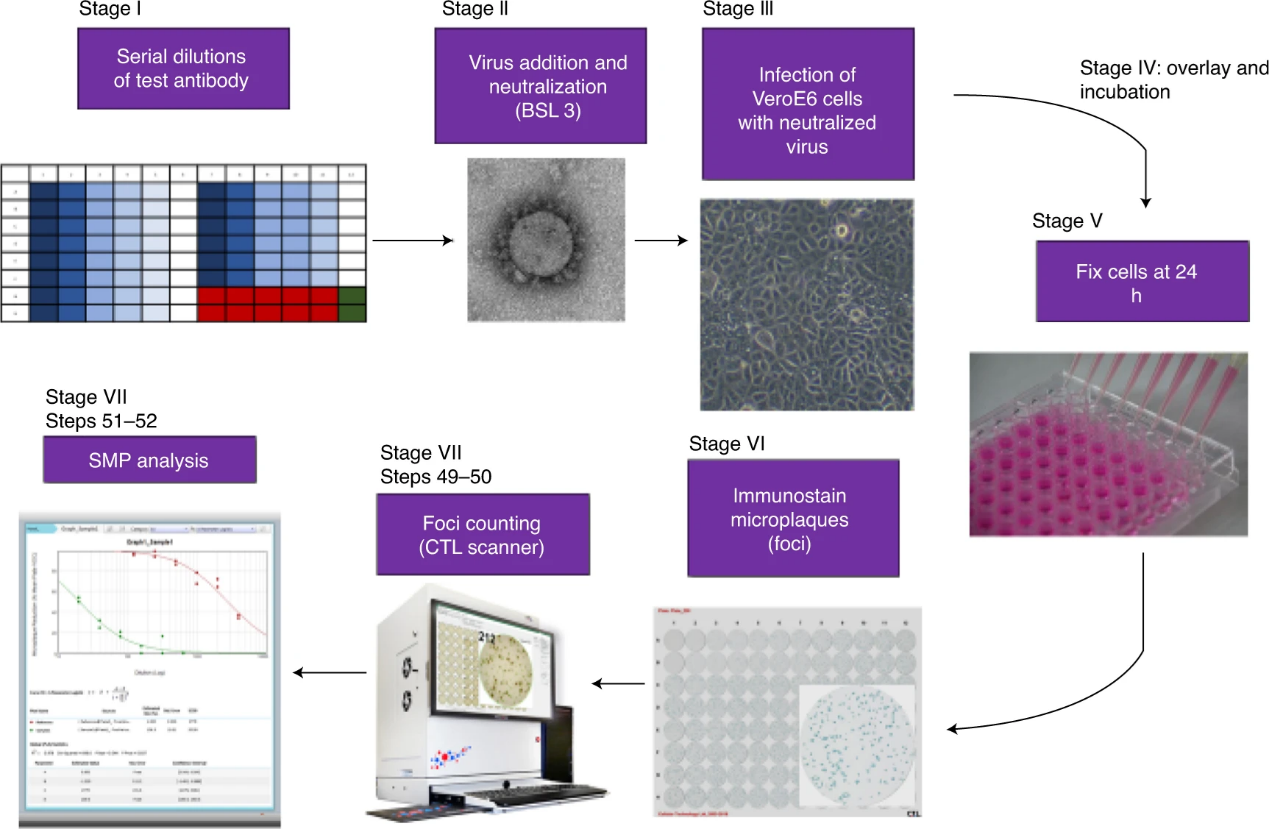
图3. 微中和检测流程图
3. 假病毒中和试验(pseudotyped virus neutralization assay,PNA)
PNA允许在较低的生物隔离条件下进行(生物安全二级实验室),同时进一步提高产量,但是只能用于测量血清或基于单克隆抗体的治疗剂的中和活性。另一个PNA的局限性是只有SARS-CoV2刺突蛋白,因此对于某些候选疫苗,PNA有可能无法与野生型试验很好地相关。
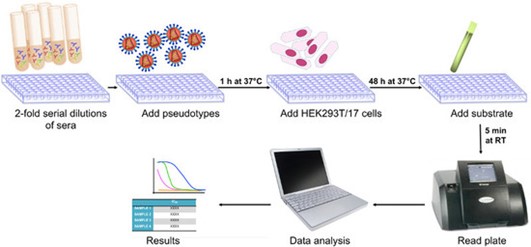
图4. 假病毒中和试验流程图
4. 基于荧光的高通量检测
患者血清被稀释以后与病毒一同孵育,再使用高内涵成像读数器定量mNG阳性细胞,该方法可以在24小时内快速检测120个样本。还具有进一步提高通量的潜力,可以容易地适应384和1536孔板。但同MNA一样,该方法目前还仅在生物科学三级实验环境下实施过。
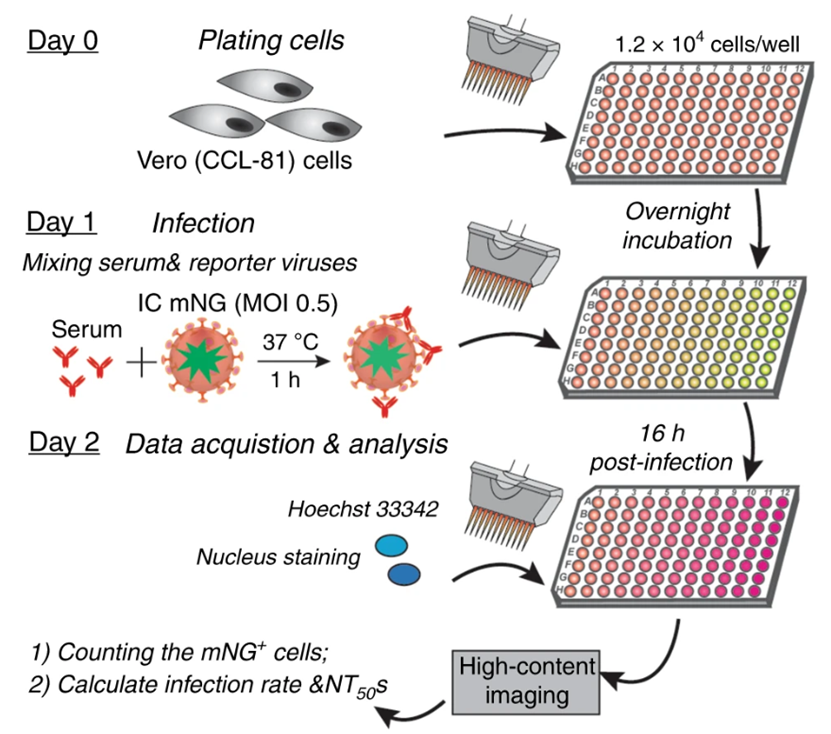
图5.基于荧光的高通量检测法
5. 侧流检测(Lateral Flow Assay,LFA)
LFA可以检测SARS-CoV-2抗原或抗体,并在15-20分钟内提供结果;结果可以直接目测或用信号检测器观察。已经开发了一种血清学抗体快速诊断试验,用于连续监测中和抗体;它可以识别对SARS-CoV-2有适应性免疫反应的个体,表明最近或以前的感染。LFA的检测物通常是COVID-19特异性IgG和/或IgM抗体。从结构上看,每个LFA都是基于一个支撑卡,分为样品垫和共轭垫。液体样本从样品垫通过毛细管作用自发地向后迁移,然后目标分析物在共轭垫形成抗原-金纳米粒子(Ag-NPs)共轭物。专用仪器,如荧光分析设备,可用于提供定性或半定量的结果。
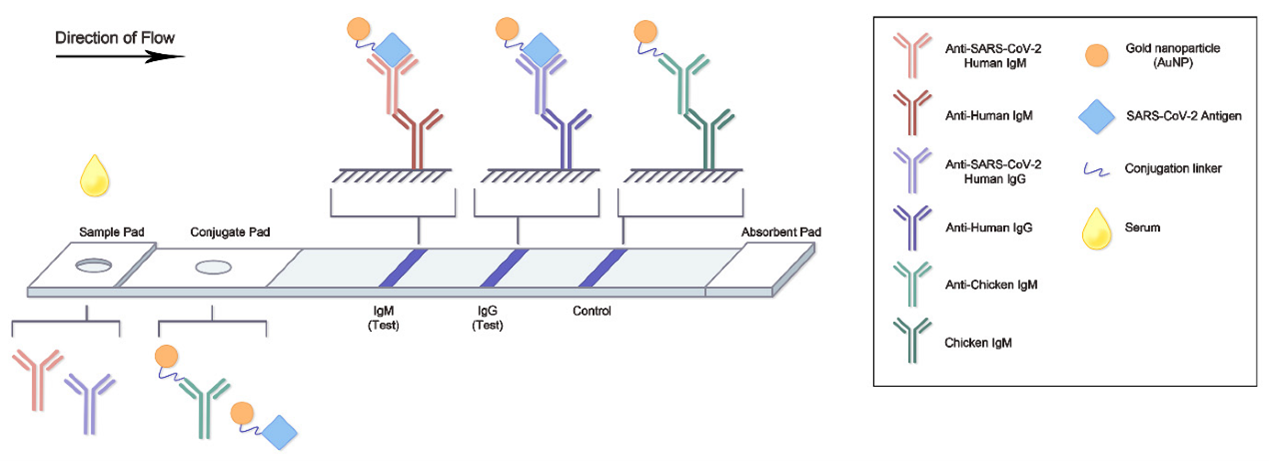
图6. 侧流检测示意图
6. 替代病毒中和测试
自 COVID-19 爆发以来,已开发了许多 ELISA 检测 SARS-CoV-2 中和抗体的方法。ELISA通常使用重组RBD蛋白或ACE2作为包被抗原,使用HRP标记的ACE2或RBD产生检测信号。使用ELISA检测中和抗原需求的生物安全等级较低且成本效益和耗时更少。

图7. ELISA检测法
7. 超敏电化学发光技术(meso scale discovery, MSD)
除了ELISA之外,MSD也可以用于检测新冠抗体,多种优势使它成为研究新冠的热门方法。它使用SULFO-TAGTM标记物,在MULTI-ARRAY和MULTI-SPORT微孔板的电极表面通电后,电化学作用激发SULFO-TAGTM标记物发出强光。MSD提供的血清学检验试剂盒可检测多种变异株抗体:
| 亚种 | 货号 | 抗原 |
| Omicron | Human LX-K15614U(IgG) LX-K15615U(IgM) LX-K15616U(IgA) LX-K15617U (ACE2) |
SARS-CoV-2 S1 RBD SARS-CoV-2 S1 RBD (B.1.1.7) SARS-CoV-2 S1 RBD (B.1.351; B.1.351.1) SARS-CoV-2 S1 RBD (BA.2; BA.2.1; BA.2.2; BA.2.3; BA.2.5; BA.2.6; BA.2.7; BA.2.8; BA.2.10; BA.2.10.1; BA.2.12) SARS-CoV-2 S1 RBD (BA.2.12.1) SARS-CoV-2 S1 RBD (BA.2+L452M) SARS-CoV-2 S1 RBD (BA.2+L452R) SARS-CoV-2 S1 RBD (BA.3) SARS-CoV-2 S1 RBD (BA.4; BA.5) SARS-CoV-2 S1 RBD (AY.3; AY.4; AY.4.2; AY.5; AY.6; AY.7; AY.12; AY.14; B.1.617.2; B.1.617.2+∆144) |
| Delta | Human LX-K15516U (IgG) LX-K15517U (IgM) LX-K15518U (IgA) LX-K15519U (ACE2) |
SARS-CoV-2 S1 RBD SARS-CoV-2 S1 RBD (AY.1; AY.2) SARS-CoV-2 S1 RBD (B.1.351; B.1.351.1) SARS-CoV-2 S1 RBD (B.1.1.7+E484K; P.3) SARS-CoV-2 S1 RBD (B.1.258.17; B.1.466.2) SARS-CoV-2 S1 RBD (B.1.620) SARS-CoV-2 S1 RBD (B.1.525; B.1.526; B.1.618; P.2; R.1) SARS-CoV-2 S1 RBD (AY.3; AY.4; AY.4.2; AY.5; AY.6; AY.7; AY.12; AY.14; B.1.617.2; B.1.617.2+∆144) |
| Alpha+Gamma | Human LX-K15437U (IgG) LX-K15438U (IgM) LX-K15439U (IgA) LX-K15440U (ACE2) |
SARS-CoV-2 N SARS-CoV-2 S1 RBD SARS-CoV-2 S1 RBD (B.1.1.7) SARS-CoV-2 S1 RBD (B.1.351) SARS-CoV-2 S1 RBD (P.1) SARS-CoV-2 Spike SARS-CoV-2 Spike (B.1.1.7) SARS-CoV-2 Spike (B.1.351) SARS-CoV-2 Spike (P.1) |
(如需更多信息请联系我们)
参考文献
- What are Neutralizing Antibodies?
- Herrlein, M.-L.; Hein, S.; Zahn, T.; Mhedhbi, I.; Raupach, J.; Husria, Y.; Benz, N.I.; Eisert, J.; Bender, D.; Haberger, V.; Hastert, F.D.; Henss, L.; Schnierle, B.S.; Stingl, J.C.; Dreher, M.; Hildt, E. Comparative Investigation of Methods for Analysis of SARS-CoV-2-Spike-Specific Antisera.
- Ferrara, F.; Temperton, N. Pseudotype Neutralization Assays: From Laboratory Bench to Data Analysis.
- Muruato, A.E., Fontes-Garfias, C.R., Ren, P. et al. A high-throughput neutralizing antibody assay for COVID-19 diagnosis and vaccine evaluation.
- Liu, K.-T.; Han, Y.-J.; Wu, G.-H.; Huang, K.-Y.A.; Huang, P.-N. Overview of Neutralization Assays and International Standard for Detecting SARS-CoV-2 Neutralizing Antibody







 沪公网安备31011502400759号
沪公网安备31011502400759号
 营业执照(三证合一)
营业执照(三证合一)


