国自然作为每个临床及科研人员历年必争之地,它的地位不言而喻。而国自然所青睐的选题是需要符合国家科学研究需求的,所以申请国自然要去靠近热点才会有好的效果(见图1)。今天,我们就一起来分析下国自然热点中的“细胞衰老”。
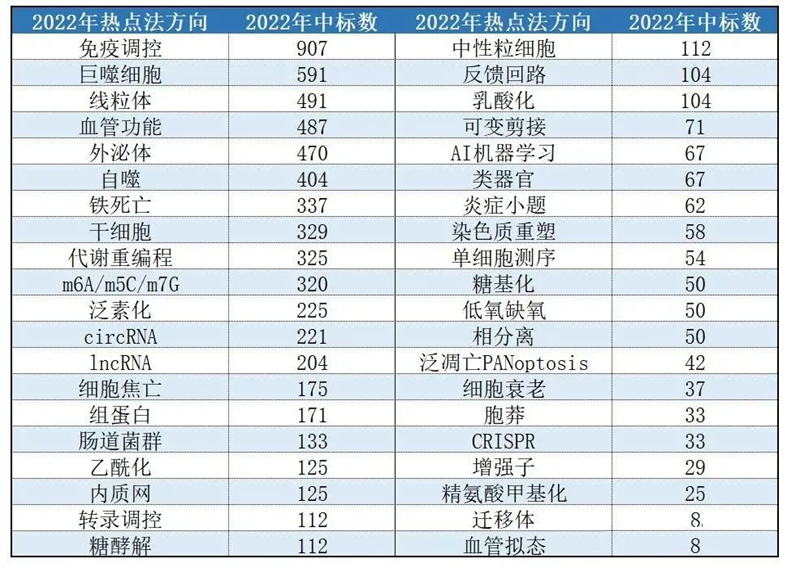
图1.2022年国自然热点方向
从科学家发现细胞寿命有限距今不过半个世纪,衰老的源头还在摸索,作为近几年兴起的研究领域,“细胞衰老”在国自然申请中越来越占据优势,通过对近十年有关细胞衰老基金项目的统计,可以发现项目数量是一个逐年递增的趋势,所以对于细胞衰老仍是一个研究的热点。
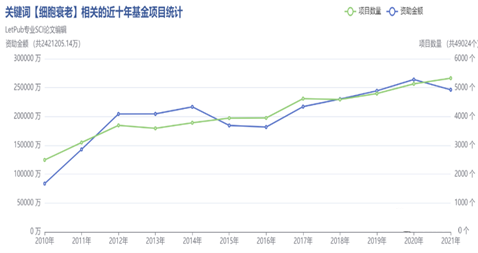
图2.细胞衰老领域国自然申请情况
一、什么是细胞衰老?
在聊细胞衰老之前,我们先来聊一聊什么是衰老?严谨的衰老定义,应该既考虑微观(细胞),也考虑宏观(器官/系统),在生物学名著《衰老生物学》中,作者认为,随着衰老起因的研究越来越多,衰老的定义可以被修正为:“衰老是由时间推移,以及与环境相互作用而引起的分子、细胞和机体结构与功能的随机改变,衰老增加死亡的可能性。”
细胞是生命最小的结构功能单位,细胞的衰老是组织、器官、机体衰老的基石。那什么又是细胞的衰老呢?其实细胞衰老现象最早在 1961 年被报道。因为在 1961 年,美国生物学家 Leonard Hayflick 在体外培养正常人的成纤维细胞时发现,即使给予细胞生长最适宜的条件,细胞分裂至一定代数时也会发生衰竭,从而使细胞周期进入了一种“不可逆”的停滞状态。基于此种现象,Hayflick首次提出了细胞衰老的概念,是一种永久性的细胞周期终止状态。
二、细胞衰老有几种表型?
细胞衰老是一种永久性的细胞周期终止状态,用以响应不同的损伤刺激。细胞衰老的原因主要是以下3个:DNA损伤应答(DNA damage response,DDR),DNA损伤引起DNA损伤应答,导致p53磷酸化,导致细胞周期停滞;端粒缩短和损伤,细胞因为不断地分裂,导致端粒缩短,从而诱导细胞发生衰老的现象;癌基因的激活,活化的癌基因导致活性氧(ROS)的产生,导致DNA损伤积累在脆性位点,通过DNA损伤应答导致细胞周期停滞。针对细胞衰老,目前一共有8种类型,分别是:
1.复制性细胞衰老,也就是多次分裂之后增殖能力的减少,最终导致完全停止。
2.DNA损伤诱导细胞衰老,由不可修复的DNA损伤诱导的细胞衰老。
3.致癌基因诱导细胞衰老,Ras等致癌基因的激活,或者PTEN等抑癌基因的失活能够导致细胞衰老。
4.氧化应激诱导细胞衰老,细胞代谢的氧化产物或者已知的氧化剂导致的细胞衰老。
5.化疗诱导细胞衰老,多个抗肿瘤药物能够诱导细胞衰老。
6.线粒体功能失调相关细胞衰老,线粒体功能失调导致细胞衰老。
7.表观遗传诱导细胞衰老,DNA甲基化抑制子或者组蛋白脱乙酰酶诱导细胞衰老。
8.旁分泌细胞衰老,由原代衰老细胞产生的衰老相关分泌表型(SASP)诱导。
三、细胞衰老是一把“双刃剑”
1.细胞衰老的有益作用
细胞衰老是一种进化过程中发挥一些基本功能及有益功能的应激反应(图3)。在胚胎发育中,衰老细胞表现出了明显的有益作用。细胞衰老的一种独特形式发生在哺乳动物发育中,调控其胚胎和胎盘的生长发育。同样,在两栖动物中,细胞衰老发生在发育的特定阶段以塑造身体的生长。因此,生命早期的细胞衰老对正常的发育和形态发生非常重要;而在生命后期,细胞衰老则对组织修复和抑制肿瘤生长起重要作用。虽然肿瘤抑制活性主要由细胞自主性细胞周期停滞介导,但大多数其他衰老功能均涉及SASP。随着时间的积累,尽管SASP有利于组织的正常发育与修复,及免疫细胞的募集;但其持久的SASP作用可能会引发慢性炎症,并导致衰老相关疾病甚至会引起癌症。
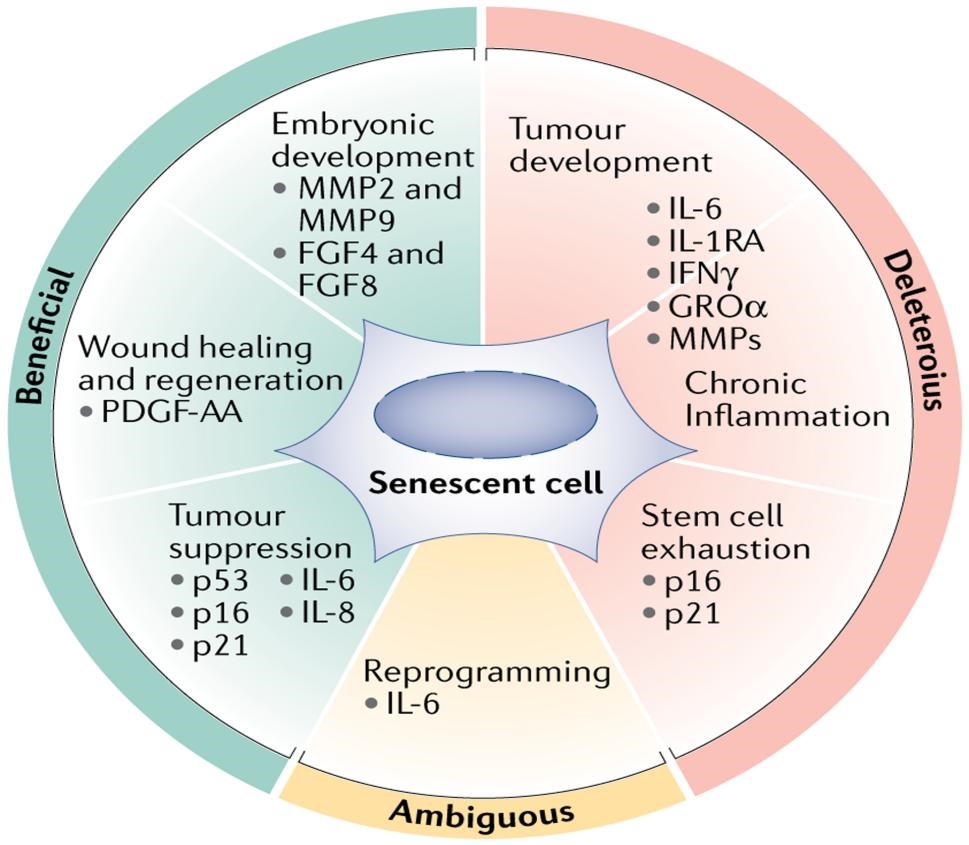
图3.细胞衰老的生物学结果
2.细胞衰老的有害作用
衰老细胞能够通过多种机制促进机体的衰老。随着年龄的增长,个体往往会表现出高循环水平炎症分子的状态(即炎症)。炎性衰老是各种衰老相关的慢性疾病的一个风险因素,包括心血管疾病、一些癌症和神经退行性疾病,并且还与过早死亡相关。此外,老年人血液中的炎症分子还与体重减轻、肌肉萎缩、身体虚弱、慢性炎症和抑郁相关(这些症状被认为是身体机能下降的表现)。在探究衰老相关慢性表型的共同基因组变异时,研究人员揭示了细胞衰老、炎症和身体机能下降之间的分子联系。事实上,IL-6、IL-1、IL-1RA和肿瘤坏死因子(tumour necrosis factor,TNF)受体等所有重要的SASP效应因子在血液中浓度升高均可作为预测老年人慢性疾病的依据。在小鼠体内移植相对较少的衰老细胞,即会导致组织功能障碍和寿命缩短。这可以证明细胞衰老是导致身体机能下降和衰老相关疾病的原因。
四.细胞衰老现象与肿瘤关系
肿瘤的典型性特征之一就是持续的分裂和增殖的能力。而细胞衰老过程却恰恰使细胞永久性地退出细胞周期。因此,很早之前,就有研究人员认为细胞衰老是防止细胞发生癌变的第三道保障。第一道保障是细胞内 DNA 的损伤修复机制;第二道保障是诱导细胞凋亡的能力;第三道保障是诱导细胞发生衰老。所以长久以来,大多数的研究人员都认为细胞衰老对于肿瘤发生具有抑制作用。
1.细胞衰老对于肿瘤发生的抑制作用
细胞衰老是现在研究得很热门的一种抗癌机制。细胞衰老过程中,Rb 和 p53 蛋白在诱导细胞发生衰老时起到了至关重要的作用。而 Rb 蛋白和 p53 蛋白又是非常关键的抑癌基因,抑制了细胞发生癌变的过程。很多肿瘤的发生都是由于抑癌基因的失活而导致的。研究表明,Rb 和 p53 蛋白的活性增强,可以启动细胞进入衰老过程。因此,如果细胞要发生癌变,那么规避衰老现象是细胞发生癌变的必要条件。因此,现在越来越多的研究,开始关注如何启动细胞衰老现象从而抑制肿瘤的发生发展。有研究发现,在 PTEN 基因失活的小鼠前列腺模型中,可以在癌前病变的小鼠组织中检测到细胞衰老现象,但是在发生了恶性前列腺癌的小鼠组织中却没有检测到细胞衰老现象。而这种差异的关键在于 p53 信号是否激活。另有研究发现,在小鼠模型中高表达 K-Rasv12 癌基因,可以诱导癌前病变、多发腺瘤,甚至是恶性的腺癌。在癌前病变和腺瘤组织中可以检测到细胞衰老,以及 p16、Dec1 以及 HP-1 等衰老标志分子,但是在腺癌细胞中不能检测到细胞的衰老现象。这些研究结果都提示激活的癌基因在小鼠体内诱导细胞衰老,但是由于少数细胞内的突变积累导致极少数的细胞突破了衰老防线,并进一步发展为恶性肿瘤。
2.细胞衰老对于肿瘤发生的促进作用
尽管上述的研究表明,体内的衰老现象是一种重要的抗肿瘤防卫机制,但是由于衰老细胞仍然保留基本的细胞代谢过程,同时发生衰老的细胞可以产生各种活性蛋白和细胞因子(也就是 SASP 现象)也可能对肿瘤发生产生了促进的作用。衰老细胞可以不断积累产生各种细胞炎性因子以及上皮生长因子,从而对衰老细胞周围的微环境的结构和功能造成了破坏,因此衰老细胞可以通过 SASP 现象而间接地对细胞造成损伤,甚至诱导细胞恶性增殖并发生癌变。衰老不足可能引起肿瘤的发生,但是过度地衰老也可以导致肿瘤的发生。
五、细胞衰老检测指标有哪些?
细胞衰老的特征包括细胞形态变化、细胞周期阻滞和氧化应激水平。体外衰老表型的确定往往需要多个特征同时验证, 有研究至少验证 3 个不同的特征。接下来会分别介绍有关形态学变化、细胞周期、细胞抗氧化能力相关的检测指标。
1.与形态变化有关的指标
衰老相关的β-半乳糖苷酶活性,SA-β-Gal 活性升高被一致认为是评价细胞衰老的生物学标志,它会随着细胞的衰老而累积增多;
观察细胞形态的变化,衰老的细胞它的形态特征是体积会明显增大, 如果是生长在固相载体表面时明显呈现扁平状, 细胞核增大且形状不规则,核纤层蛋白 B1 (lamin B1)是维持细胞核结构完整性的关键, 其减少导致核完整性和稳定性下降, 继而导致其他核变化, 这种减少可以通过成像或免疫印迹检测, 从而指示体外衰老的现象。
(3)衰老的发生经常与持续性的 DNA 损伤反应(DNA damage response, DDR)有关,同时伴随着细胞分泌功能增加, 即衰老相关分泌表型(SASP),TNF-α、IL-1α、IL-1β、IL-6、IL-8、基质金属蛋白酶(MMP)等SASP相关因子以及HMGB1的核定位缺失也是常用的衰老标志物。
2.与细胞周期相关的指标
1.常用的衰老标志物,是与衰老相关的细胞周期停滞有关的分子,比如细胞周期蛋白依赖性激酶抑制分子p16 INK4A或p21Cip1等,用于显示持久性DNA损伤灶的 DNA修复蛋白53BP1或YH2A.X,还有增殖标记物Ki67的缺乏。
目前,检测细胞衰老还没有一个通用的标记物。由于衰老细胞表达的标志物会随着衰老刺激、细胞类型、刺激时间有所变化,所以研究人员如果要证实细胞衰老的表型,必须同时评估几种与衰老有关的标记物。
3.细胞抗氧化能力相关指标
可以通过检测活性氧(reactive oxygen species, ROS)在体内的含量,因为ROS的堆积, 会导致氧化损伤, 从而引发衰老及相关疾病,除此之外,超氧化物歧化酶(superoxide dismutase, SOD)是清除ROS 的关键酶, 可以将毒性超氧化物转化为过氧化氢和水。所以SOD 也是机体抗氧化能力的重要评价指标。
综上所述,细胞衰老是一个普遍的过程,在组织重塑、伤口修复、胚胎发生中发挥重要作用。此外,衰老的异常调节常常会引起老化相关疾病及肿瘤进展,而几种细胞衰老的生物标志物,比如p16 和 p21,都是近年科研研究领域的明星分子。针对衰老的一些临床开发药物也逐步步入临床试验,或对改善人类疾病有促进作用,所以对于细胞衰老的研究还有待进一步深入。
参考文献
Childs, B.G., et al., Cellular senescence in aging and age-related disease: from mechanisms to therapy. Nat Med, 2015. 21(12): p. 1424-35.
Aunan, J.R., et al., Molecular and biological hallmarks of ageing. Br J Surg, 2016. 103(2): p. e29-46.
3.Di Micco R, et al. Cellular senescence in ageing: from mechanisms to therapeutic opportunities.Nat Rev Mol Cell Biol. 2021 Feb;22(2):75-95.







 沪公网安备31011502400759号
沪公网安备31011502400759号
 营业执照(三证合一)
营业执照(三证合一)


