近年来,随着生物技术和分析方法的不断进步,定量蛋白质和基因水平的研究在理解疾病机制和寻找治疗靶点等领域扮演着至关重要的角色。此外,深入了解组织生物学也需要考虑到空间维度的因素,因此空间分析在该领域的发展备受关注。Nature Methods杂志将空间多组学技术列为2022年最令人期待的七项技术之一,目前已有多家企业推出了空间多组学技术的商业化产品,有助于研究人员探索空间转录组的奥秘。
Nanostring GeoMx DSP技术提供结合了组织影像分析技术和高通量分子定量技术,能够在组织切片原位实现多靶标蛋白和全转录组的空间原位表达谱分析。通过捕获具有形态学背景的图像,按照组织形态、表型、单个细胞、按网格或者绘制区域轮廓,研究者可以选择感兴趣的区域进行分析。
整个组织切片、FFPE 或新鲜冷冻切片均可成像并进行 RNA 或蛋白质染色。然后,研究人员可以根据生物学特性精确选择要分析的组织区块或细胞类型,并随后使用 nCounter分析系统或Illumina测序仪计算表达水平。
基本原理
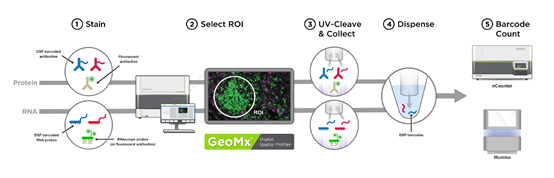
DSP Workflow全流程
1、标记荧光抗体与待测指标共孵育:一张5μm厚度的切片同时用成像试剂(荧光标记的抗体/探针)和定量试剂(Oligo标记抗体/探针)混合杂交
2、ROI区域圈选:可以选择任何区域,任何形状和大小的ROI
3、区域划分&紫外光解DSP Barcode:每个圈选的目标区域依次被紫外光照射,并切断定量试剂上偶联的Oligo序列。在不接触样本的情况下,用微毛细管快速吸出解离的Oligo序列,使样本切片完整。
4、逐个ROI收集DSP Barcode到96孔板: Oligo标签被收集到96孔收集板中,每一个孔对应组织切片上选择的一个ROI/AOI。
5、Barcode计算、测序和数据分析:收集的Oligo利用高通量测序(NGS)或 在NanoString的nCounter平台上进行定量。
优势
技术优势
- Proteins & RNAs 组织原位表达,从靶向蛋白到全转录组分析方案
- 兼容FFPE石蜡包埋样品,实现高靶点+高灵敏度分析
- 灵活、精准的区域(ROIs)选择和自动化富集细胞群
- 应对多种应用场景
- 预先验证的Panel&客制化方案
样本类型
穿刺样品、FFPE石蜡包埋样品、组织阵列样品(TMA)、新鲜/冻存样品、固定切片
应用领域
- 肿瘤/肿瘤免疫:肿瘤异质性/分型、肿瘤耐药机制、肿瘤转移机制、肿瘤免疫微环境、免疫治疗、化疗预后标志物发现
- 免疫学/感染科学:感染组织原位免疫反应关系、治疗、预后靶点发现和验证、感染和组织损伤、肿瘤发生的关系、感染的分子病理图谱分析
- 神经科学:神经系统细胞群组织原位分布和相互作用机制、神经退行性疾病、神经系统肿瘤、神经系统感染
- 组织疾病:器官组织异质性、组织器官亚结构分析和疾病关系、组织疾病精细分子病理图谱
- 发育生物学:器官亚结构发育分子机制、发育类疾病相关的分子生物学通路的研究
服务列表
|
服务类型 |
种属 |
Panel说明 |
|
NGS平台蛋白质检测 |
人,小鼠 |
使用NGS 平台在空间水平同时分析10 到 140 个蛋白质目标。核心包含4个基础靶标和必要的阳性、阴性对照,最多可以添加14个模块。 |
|
核心 |
CD45、Ki67、CD31、Beta-2microglobulin(Human)、GFP(mouse)、6 controls |
|
|
模块 |
免疫细胞类型、IO肿瘤药物靶标、免疫激活状态、泛肿瘤、细胞死亡、MAPK信号通路、PI3K/AKT信号通路、髓系细胞、神经细胞类型、AD病理学、AD病理学拓展、PD病理学、神经胶质细胞亚型、细胞自噬 |
|
|
人全转录组图谱(WTA) |
人 |
人全转录组图谱覆盖人的全转录组,可以在在单个组织切片中同时分析 18,000 多个基因的 RNA 表达。 |
|
小鼠全转录组图谱(Mu WTA) |
小鼠 |
小鼠全转录组图谱覆盖所有小鼠品系的全转录组,可以在在单个组织切片中同时分析21,000 多个基因的 RNA 表达。 |
|
癌症转录组图谱(CTA) |
人 |
癌症转录组图谱用于对肿瘤生物学、肿瘤微环境和免疫反应进行全面分析,可以在在单个组织切片中同时分析 1,800 多个基因的RNA表达。 |
|
犬癌症图谱 |
犬 |
犬癌症图谱用于研究犬对癌症以及免疫生态学治疗的免疫反应,可以在单个组织切片中同时分析1,962多个基因的 RNA 表达。 |
|
空间多组学数据分析 |
不限 |
提供标准化及定制化数据分析,包括箱型图、散点图、火山图、条形图等多种展示 |
结果展示
数据分析:提供多种数据视图,包括箱型图、散点图、火山图、条形图等
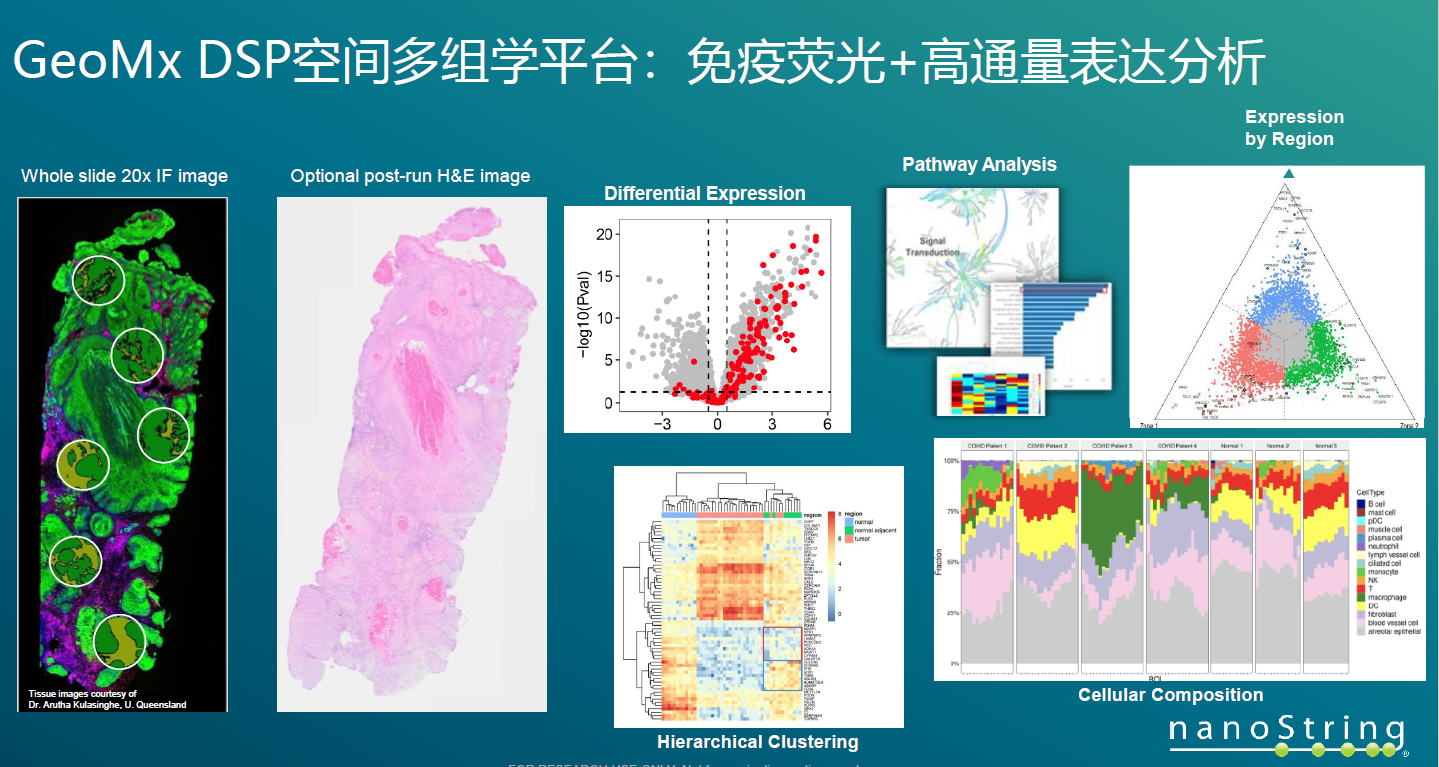
应用案例
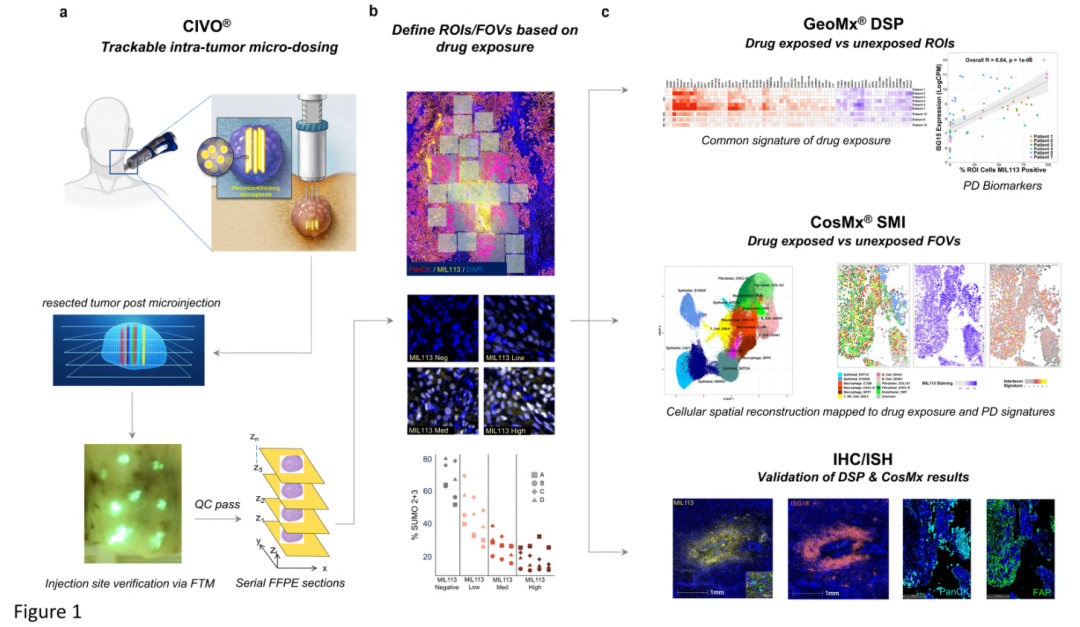
Trackable Intratumor Microdosing and Spatial Profiling Provide Early Insights into Activity of Investigational Agents in the Intact Tumor Microenvironment
Clin Cancer Res. doi: 10.1158/1078-0432.CCR-23-0827.
研究者为了构建再现TME复杂性的药物评估模型,结合CIVO和空间生物读数,在CIVO瘤内微剂量给药及追踪之后,基于药物暴露确定感兴趣的区域(ROIs)。利用GeoMx® DSP空间全转录组技术在空间定义的感兴趣区域对药物暴露区(n=214)和未暴露区(n=140)进行全面比较,发现TAK-981暴露的局部组织区域表现出了SUMO通路抑制、I型IFN反应增强和细胞周期抑制。通过CosMx™ SMI单细胞空间原位分析成像技术进行单细胞分辨率的特征评估,发现subasumstat 显著改变了TME内特定免疫细胞和基质细胞的活性状态,包括肿瘤相关巨噬细胞、成纤维细胞和T细胞。结合IHC/ISH对结果进行验证,最终成功构建可以用于评估药物作用机制的空间模型。
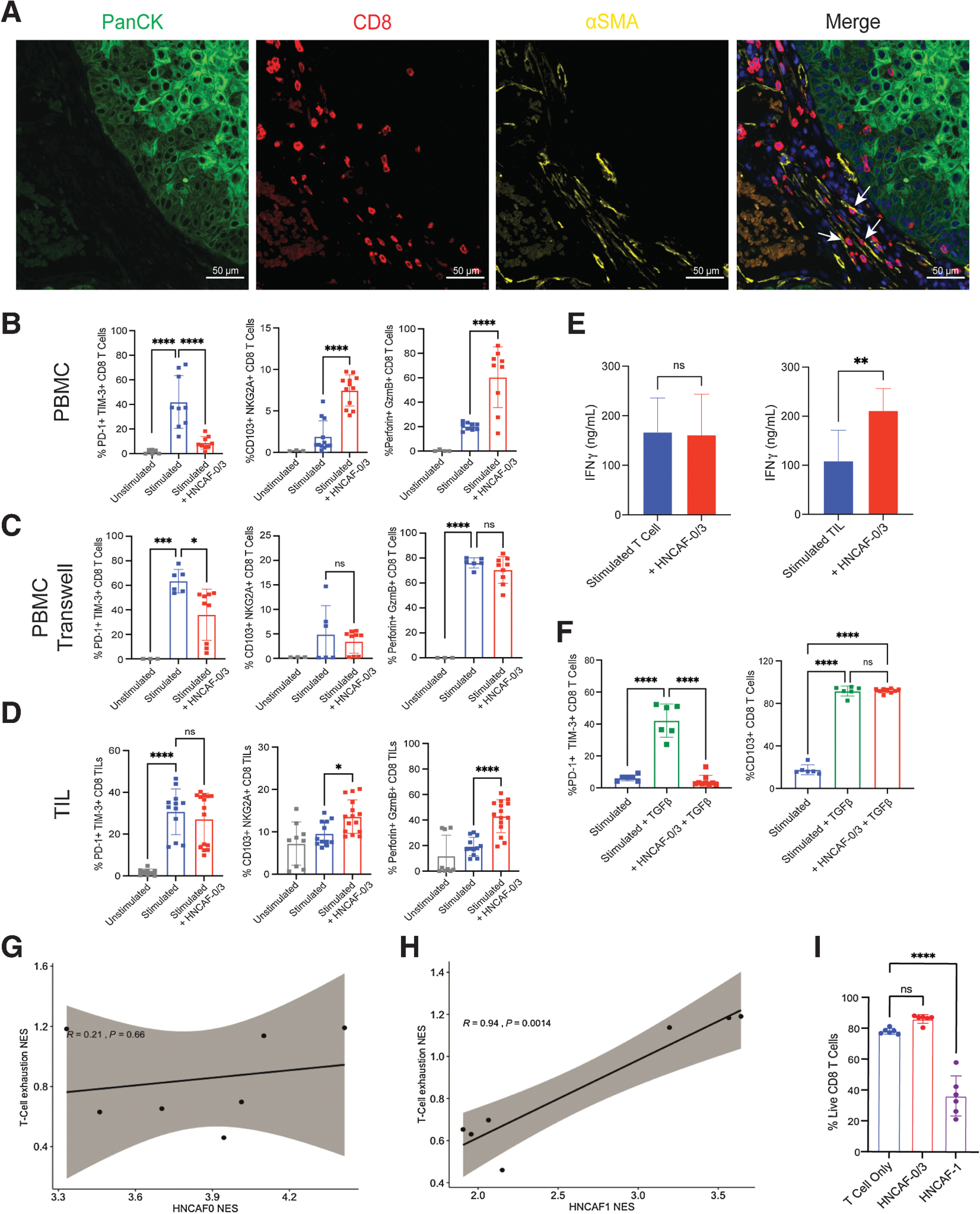
Immunostimulatory Cancer-Associated Fibroblast Subpopulations Can Predict Immunotherapy Response in Head and Neck Cancer
Clin Cancer Res doi: 10.1158/1078-0432.CCR-21-3570.
研究者对接受 αPD-1 疗法 nivolumab 治疗的晚期头颈鳞状细胞癌患者的新辅助试验中的 4 名患者的治疗前和治疗后肿瘤进行采样。使用scRNA-seq 纵向分析人类 HNSCC 的治疗前和治疗后对照组,生成人类 HNSCC TME 的动态图谱,识别了HNSCC 微环境中功能独特的 CAF 群体。之后通过DSP技术对患者的免疫基因组表达进行分析。使用抗CD8、抗αSMA、抗PanCK和DAPI染色剂进行形态学鉴定。
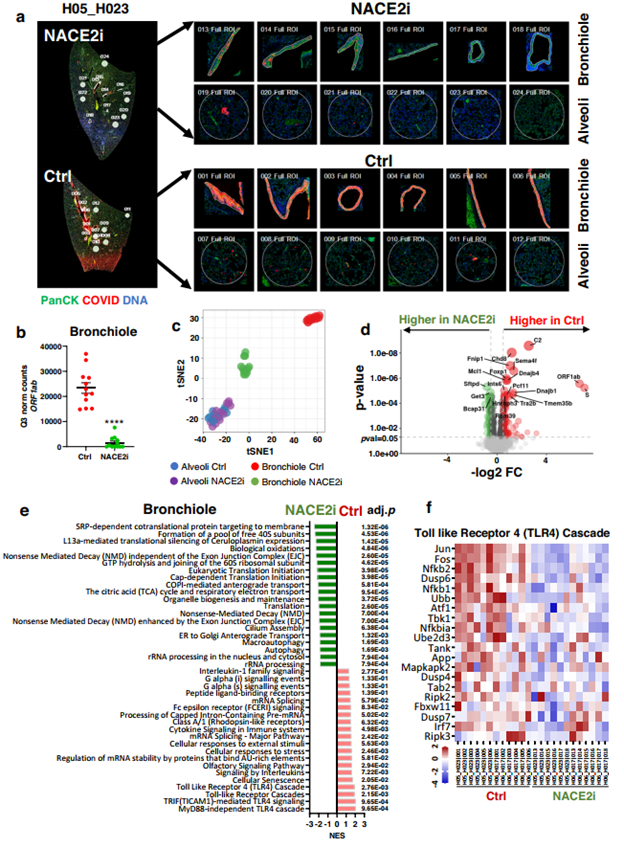
In vivo inhibition of nuclear ACE2 translocation protects against SARS-CoV-2 replication and lung damage through epigenetic imprinting
Nature communications doi: 10.1038/s41467-023-39341-4.
研究人员利用GeoMx®空间全转录组技术对SARS-CoV-2感染的黄金仓鼠的肺组织进行了深入分析,通过研究组织特异性的转录组特征和不同区域的病毒载量差异,发现了一种具有特异性和选择性的核ACE2抑制剂 — NACE2i,并确定了NACE2i所诱导的肺部炎症缓解相关的转录组表达特征。发现该抑制剂可以在感染2天后抑制病毒复制,并且能够预防COVID-19引发的早期肺部炎症、组织病变和巨噬细胞浸润,增加支气管小叶中NK细胞的浸润。







 沪公网安备31011502400759号
沪公网安备31011502400759号
 营业执照(三证合一)
营业执照(三证合一)


